سلام به همه دوستان خوبم. حتمأ بعد از مطالعه آموزش فصل دوم شیمی یازدهم در سایت بخون از خودتان میپرسید جواب خود را بیازمایید، پیوند با ریاضی و با هم بیندیشیم و … را از کجا میتوانم پیدا کنم؟ نگران نباشید درمقاله گام به گام فصل دوم شیمی یازدهم جواب تمامی سوالات کتاب درسی شیمی یازدهم و تمرینهای دورهای آخر فصل به طور کامل و به صورت تشریحی داده شده است.
حتمأ میدانید که در بودجهبندی کنکور، شیمی یازدهم بیشترین تعداد تست را به خود اختصاص داده است؛ بنابراین حل درست سوالات و تمرینهای این فصل و فصلهای دیگر واجب و ضروری میباشد. پس با من تا انتها مقاله همراه باشید تا پاسخ کامل تمام سوالات را در کمترین زمان ممکن بدون نیاز به منابع دیگر بیابید.
اگر آموزش فصل دوم شیمی یازدهم را هنوز مطالعه نکردهاید، پیشنهاد میکنم از طریق کلیک روی لینک وارد آن شوید و به تمام نکات مهم فصل دو شیمی یازدهم دسترسی پیدا کنید. همچنین برای بهرهمندی از آموزش رایگان سایر فصلها به لینک آموزش شیمی یازدهم بروید. در ضمن میتوانید پی دی اف همین مقاله را در انتها دانلود کنید تا هر وقت آن را لازم داشتید به آن مراجعه کنید.
جواب خو را بیازمایید شیمی یازدهم صفحه 51
جدول زیر، سرانە مصرف سالانه برخی مواد خوراکی را نشان میدهد. با توجه به آن، به پرسشهای مطرح شده پاسخ دهید.
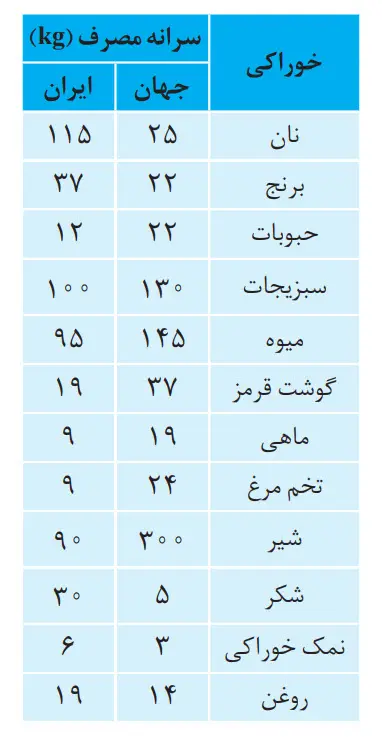
الف) دیابت بزرگسالی یکی از بیماریهای شایع در ایران است. مصرف بیرویە کدام مواد در گسترش این بیماری نقش دارد؟
برنج – شکر – نان
ب) گوشت قرمز و ماهی افزون بر پروتئین، محتوی انواع ویتامین و مواد معدنی است. چه پیشنهادهایی برای گنجاندن آنها در برنامە غذایی خانواده خود دارید؟
با تنوع بخشیدن به غذاهای حاوی گوشت و مصرف آنها در طول هفته
پ) شیر و فراوردههای آن، منبع مهمی برای تأمین پروتئین و بهویژه کلسیم است. کارشناسان تغذیه برمصرف مناسب آنها برای پیشگیری و ترمیم پوکی استخوان تأکید دارند. اگر شما یک مدیر تصمیمگیرنده در کشور باشید، چه راهکارهایی برای افزایش مصرف آنها ارائه میکنید؟
کاهش قیمت، توزیع آن در مدارس و محل کار کارمندان، فرهنگسازی و تشویق خانوادهها به مصرف شیر با برنامهسازی و….
ت) کارشناسان تغذیه بر مصرف حبوبات مانند نخود، لوبیا، عدس و… در برنامە غذایی تأکید دارند زیرا سرشار از مواد مغذی هستند. براساس برنامە غذایی خانواده خود چه پیشنهادی برای افزایش مصرف آنها دارید؟
با تنوع بخشیدن به غذاهای حاوی حبوبات استفاده از حبوبات در کنار سالادها و یا عصرانه
اگر به دنبال منبعی مناسب برای ترجمه درس های عربی یازدهم و همچنین حل تمرین های عربی یازدهم هستید، حتما لینک معنی درس های عربی یازدهم و معنی درس های عربی یازدهم را باز کنید تا کاملترین ترجمه را از درس های عربی یازدهم و پاسخ تمرینات این پایه داشته باشید.
پاسخ کاوش کنید صفحه 53 شیمی یازدهم
درباره «اثر نوع و مقدار ماده بر انرژی آن» کاوش کنید.
وسایل و مواد مورد نیاز: چراغ الکلی یا شمع، لولۀ آزمایش بزرگ، دماسنج، پایه، میله، گیره، انبر، ماکارونی و مغز گردو.
هشدار: از عینک امینی استفاده نموده و نکات ایمنی را هنگام کار با چراغ بونزن رعایت کنید.
- یک لولە آزمایش بزرگ را با گیره به پایه و میله وصل کنید.
- درون آن تا 60 میلی لیتر آب بریزید و دمای آن را اندازهگیری کنید (توجه داشته باشید که دماسنج با بدنه یا ته لوله تماس نداشته باشد.
- یک گرم یا مغزگردو بردارید و آن را با انبر یا میله نازک تا شعلهورشدن روی شعله بگیرید. بلافاصله آن را تا سوختن کامل زیر لولە آزمایش نگهدارید. پس از سوختن کامل و خاموششدن شعله، دمای پایانی آب را یادداشت کنید.
- آزمایش را جداگانه با دو گرم یا مغز گردو و همچنین با دو گرم ماکارونی تکرار و جدول زیر را کامل کنید سپس به پرسشهای مطرح شده پاسخ دهید.
الف) با توجه به این که در آزمایش 1 و 2، نوع مادهای که میسوزد یکسان است، چرا تغییر دمای آب متفاوت است؟
زیرا جرم ماده در دو آزمایش متفاوت است.
ب) با توجه به این که در آزمایش 2 و 3، مقدار مادهای که میسوزد یکسان است، چرا تغییر دمای آب تفاوت دارد؟
زیرا نوع ماده در دو آزمایش متفاوت است.
ث) یافتههای خود را از این آزمایش جمعبندی کنید؟
گرمای آزاد شده در سوختن هم به جرم ماده و هم به نوع ماده بستگی دارد.
جواب باهم بیندیشیم صفحه 55 شیمی یازدهم تجربی
1- شکل زیر دو نمونه از هوای صاف شهر شما را با جرم یکسان نشان میدهد. با توجه به آن در هر مورد با خط زدن واژۀ نادرست، عبارت را کامل کنید.

الف) شکل A نمونهای از هوا را در شب نشان میدهد.
ب) شکل B نمونهای از هوا را در یک روز تابستانی نشان میدهد.
پ) اگر مجموع انرژی جنبشی ذرههای سازنده یک نمونه ماده، هم ارز با انرژی گرمایی آن باشد، انرژی گرمایی A بیشتر بوده، زیرا دمای آن بیشتر است.
2- با توجه به شکلهای زیر به پرسشهای مطرح شده، پاسخ دهید:
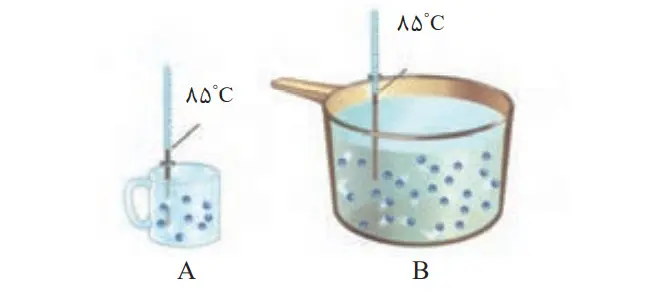
میانگین تندی مولکولهای آب را در دو ظرف مقایسه کنید.
میانگین تندی مولکولهای به دما بستگی دارد و چون دما در دو ظرف یکسان است میانگین تندی برابر است.
انرژی گرمایی آب موجود در کدام ظرف بیشتر است؟ چرا؟
B، زیرا در ظرف B مقدار ماده بیشتر است. بنابراین مجموع انرژی گرمایی ذرات بیشتر است.
جواب با هم بیندیشیم صفحه 57 شیمی یازدهم
با توجه به شکلهای داده شده، به پرسشهای زیر پاسخ دهید.
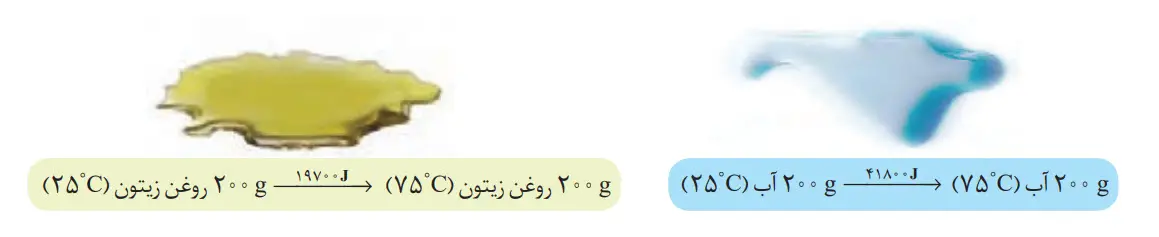
الف) توضیح دهید چرا تخممرغ در آب میپزد اما در روغن زیتون تغییر محسوسی نمیکند؟
ظرف حاوی آب برای رسیدن به دمای 75 درجه انرژی گرمایی بیشتری جذب نموده و انرژی گرمایی بیشتری دارد لذا گرمای بیشتری به تخم مرغ منتقل میشود.
ب) میدانید که ظرفیت گرمایی ماده همارز با گرمای لازم برای افزایش دمای آن به اندازە یک درجە سلسیوس است. با این توصیف ظرفیت گرمایی آب و روغن زیتون را محاسبه و با یکدیگر مقایسه کنید.
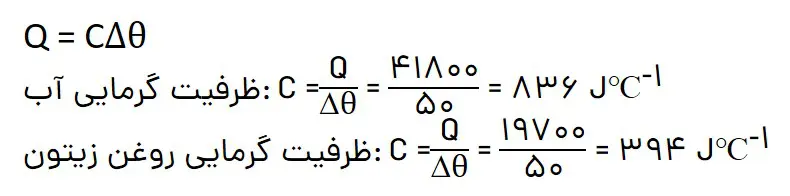
پ) ظرفیت گرمایی ماده به چه عواملی بستگی دارد؟
به جرم ماده ، نوع ماده و حالت فیزیکی بستگی دارد.
ت) در فیزیک دهم آموختید که ظرفیت گرمایی یک گرم ماده، ظرفیت گرمایی ویژه یا گرمای ویژه ( c )آن ماده را نشان میدهد، مقدار این کمیت را برای آب و روغن زیتون حساب و باهم مقایسه کنید.
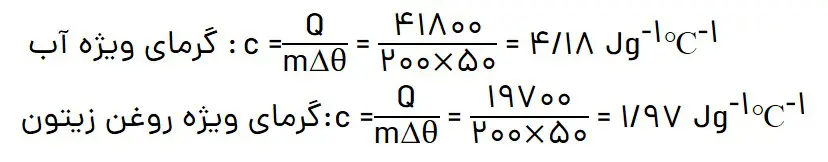
ظرفیت گرمایی ویژه آب بیشتر از روغن است.
ث) رابطهای میان ظرفیت گرمایی و گرمای ویژه یک ماده بیابید.

اگر میخواهید جواب کامل و تشریحی فعالیتهای زیست یازدهم را به صورت یکجا به دست بیاورید، کافیست تا لینک جواب فعالیتهای زیست یازدهم را باز کنید.
جواب خود را بیازمایید صفحه 58 شیمی یازدهم
1- یک استکان چای با دمای 90 C° درون اتاقی با دمای 25 C ° قرار دارد. با گذشت زمان، دما و انرژی گرمایی آن چه تغییری میکند؟ چرا؟
دما و انرژی گرمایی آن کاهش مییابد. استکان چای انرژی از دست داده و در نهایت با هوای اتاق هم دما میشود در نتیجه، میانگین انرژی جنبشی ذرات و در پی آن انرژی گرمایی چای کاهش پیدا میکند.
2- با خط زدن واژه نادرست در هر مورد، عبارت زیر را کامل کنید:
گرما را میتوان هم ارز با آن مقدار انرژی انرژی گرمایی دانست که به دلیل تفاوت در دمایی انرژی جاری میشود.
3- تکهای نان و تکهایی سیب زمینی را با جرم و سطح یکسان در دمای °C 60 در نظر بگیرید. اگر آنها را هم زمان در محیطی با دمای 29°C قرار دهیم کدام یک زودتر با محیط هم دما میشود؟ درستی پاسخ خود را در منزل بررسی کنید.
نان و سیب زمینی هر دو تقریبا از نشاسته تشکیل شدهاند بنابراین سرعت هم دما شدن با محیط به میزان آب موجود در آنها بستگی دارد. از آنجا که مقدار آب در نان کمتر است زودتر با محیط همدما میشود.
جواب باهم بیندیشیم صفحه 62 شیمی یازدهم تجربی
1- با توجه به واکنشهای زیر پاسخ دهید:
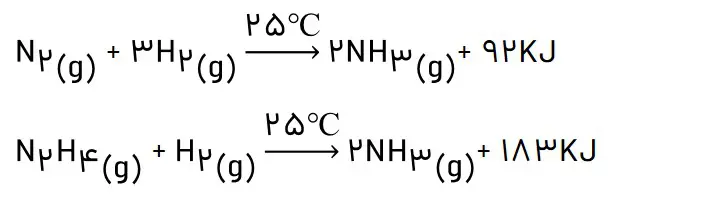
الف) چرا گرمای آزاد شده در دو واکنش متفاوت است؟ توضیح دهید.
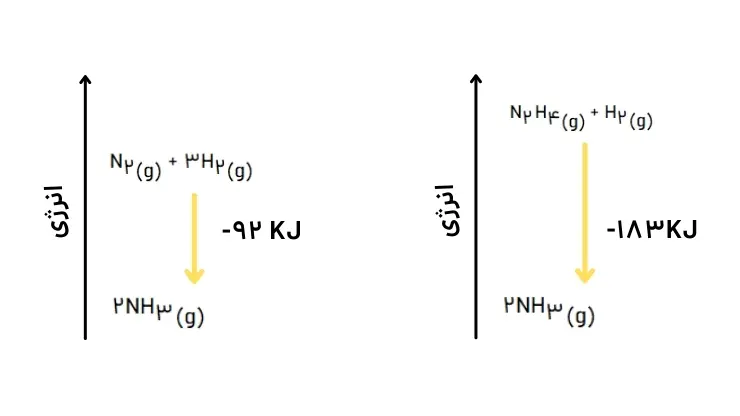
سطح انرژی پتانسیل واکنشدهندهها در دو واکنش متفاوت است لذا اختلاف سطح انرژی فرآورده و واکنشدهندهها در دو واکنش متفاوت خواهد بود.
ب) در کدام واکنش، مواد واکنشدهنده پایدارتر است؟ چرا؟
واکنش اول، سطح انرژی فراورده در دو واکنش برابر است لذا سطح انرژی در واکنش اول یعنی نیتروژن و هیدروژن که گرمای کمتری آزاد شده پایین تراست و پایدارتر هستند.
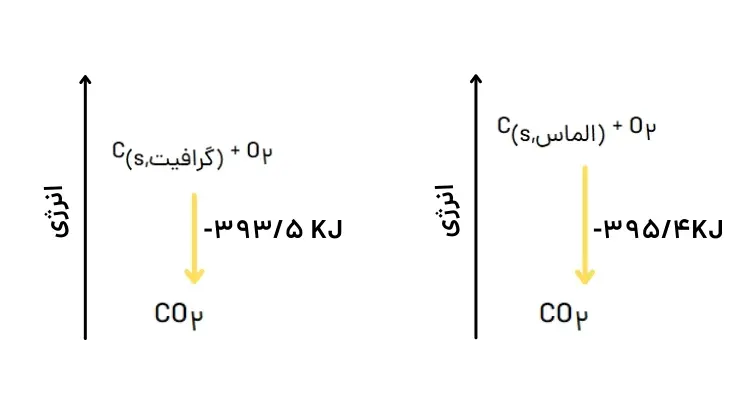
2- گرافیت و الماس دو آلوتروپ کربن هستند که فراوردە واکنش سوختن کامل آنها، گازکربندیاکسید است.
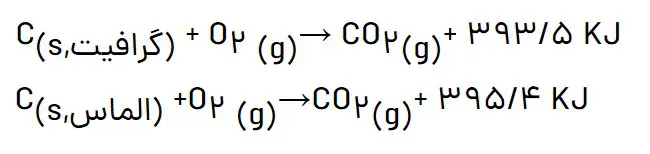
الف) چرا گرمای حاصل از سوختن یک مول گرافیت متفاوت از یک مول الماس است؟
سطح انرژی پتانسیل گرافیت و الماس با هم متفاوت و سطح انرژی فراوردهها یکسان است. به همین جهت میزان گرمای آزاد شده متفاوت خواهد بود.
ب) الماس پایدارتر است یا گرافیت؟ چرا؟
در لینک آزمایشگاه علوم تجربی یازدهم، مقالاتی وجود دارد که شامل پاسخ به همه تمرینات کتاب آزمایشگاه یازدهم میباشد، پس حتما آن را دنبال کنید.
گرافیت پایدارتر است؛ زیرا گرمای کمتری آزاد شده لذا سطح انرژِی گرافیت پایینتر از الماس است.
پ) از سوختن کامل g 2/7 گرافیت، چند کیلوژول گرما آزاد میشود؟
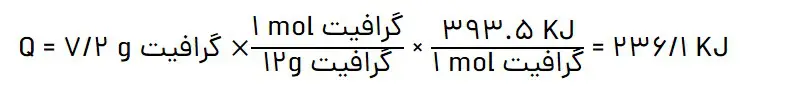
3- با توجه به گرمای واکنش داده شده، گرمای واکنش دیگر کدام است؟ ( 572KJ،-572KJ، 422KJ ،-422KJ+)؟ چرا؟
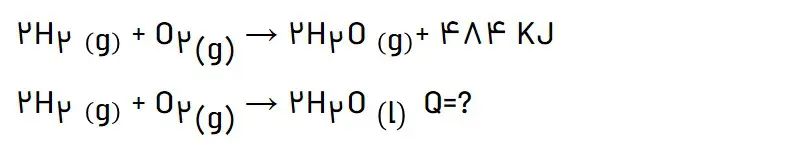
572KJ-
تفاوت دو واکنش در حالت فیزیکی فراورده است. سطح انرژی آب مایع پایینتر از آب گازی است به همین جهت گرمای بیشتری آزاد میشود.
پاسخ خود را بیازمایید صفحه 64 شیمی یازدهم
مقدار عددی ΔH، یک فرایند بزرگی آن را نشان میدهد، درحالی که علامت مثبت و منفی تنها نشاندهنده گرماگیر و گرماده بودن آن است.
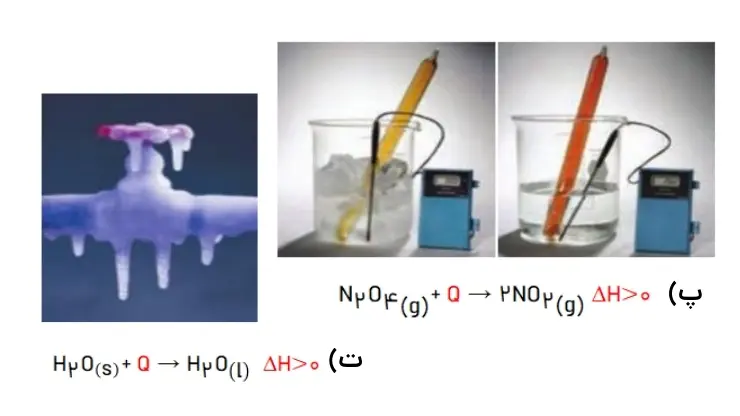
1- نماد Q را در هر معادله وارد کرده سپس علامت ΔH را در هر مورد مشخص کنید.
الف) و ب)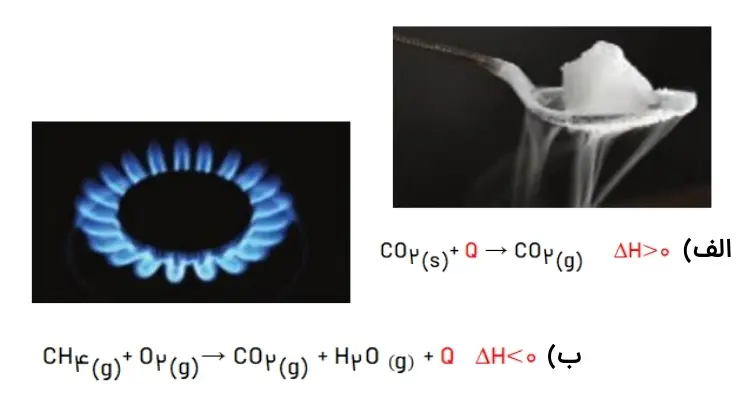
پ) و ت)
2- اگر برای تولید یک مول گاز اوزون از گاز اکسیژن، آنتالپی به اندازە 143 کیلوژول افزایش یابد، آنتالپی واکنش زیر را حساب کنید.
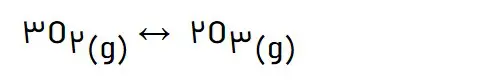
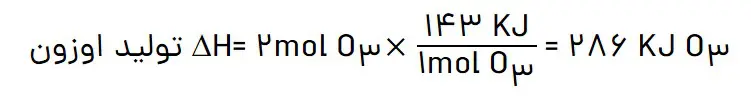
جواب خود را بیازمایید صفحه 66 شیمی یازدهم
با استفاده از دادههای جدول میانگین آنتالپی، آنتالپی هریک از واکنشهای زیر را پیشبینی کنید.
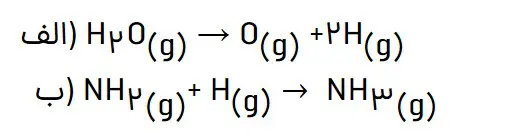
الف) با توجه به ساختار لوییس آب که دو پیوند O — H دارد، باید پیوندهای O — H شکسته شوند و اتمهای اکسیژن و هیدروژن تشکیل شوند.
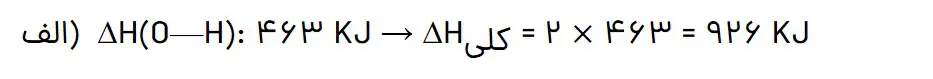
ب) با توجه به ساختار لوییس NH3 یک پیوند N—H تشکیل میشود؛ یعنی برای تبدیل NH2 به NH3 یک پیوند تشکیل میشود.
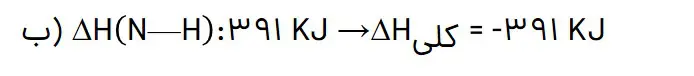
جواب خودرابیازمایید شیمی یازدهم فصل دوم صفحه 67
1- دانشآموزی برای تعیین آنتالپی یک واکنش گازی از رابطه زیر استفاده کرده است، درستی این رابطه را بررسی کنید.

هر واکنش را میتوان جمع دو واکنش دانست در واکنش اول تمام پیوندها شکسته میشود، پس آنتالپی آن مثبت و گرماگیر است. در واکنش دوم از تمام اتمها فرآوردهها بدست میآیند، که آنتالپی آن منفی و گرماده است. بنابراین مجموع آنتالپی این دو واکنش، آنتالپی واکنش مورد نظر است.
2- با استفاده از جدول میانگین آنتالپی پیوندها، H∆ هر یک از واکنشهای ترموشیمیایی زیر را حساب نموده و با H∆ داده شده مقایسه کنید.
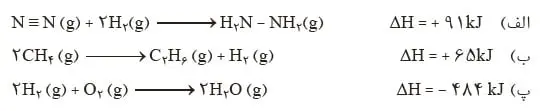
جواب سوال 2:
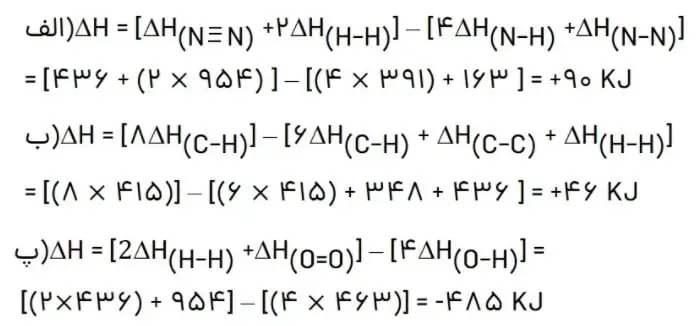
جواب خود را بیازمایید صفحه 69 شیمی یازدهم
1- هر ساختار زیر یک ترکیب آلی موجود در آن ادویه را نشان میدهد. گروههای عاملی موجود در هر مولکول را مشخص کنید و نام آنها را بنویسید.
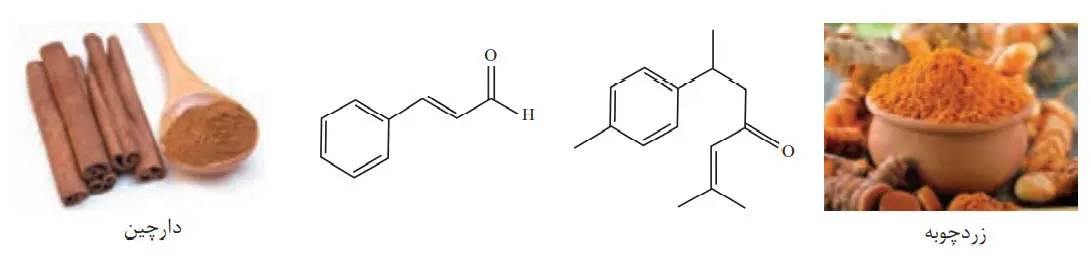
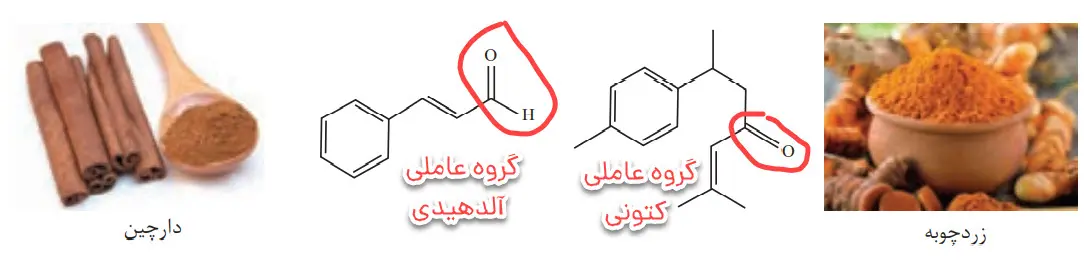
2- با توجه به ساختار ترکیبهای آلی زیر به پرسشهای مطرح شده پاسخ دهید.
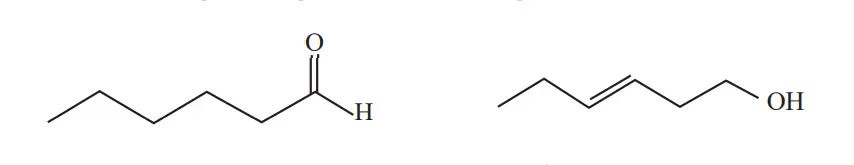
اگر به دنبال منبعی خوب برای آموزش فیزیک هستید، مقاله آموزش فصل اول فیزیک یازدهم | الکتریسیته ساکن را مطالعه کنید تا کلی نکات کلیدی در رابطه با این فصل نصیبتان شود.
الف)شمار و نوع اتمهای سازنده آنها را با یکدیگر مقایسه کنید.
اتمهای اکسیژن، هیدروژن و کربن در این ترکیبات موجود میباشد.
نوع و تعداد اتمها در دو ترکیب مشابه است. چنین ترکیباتی که نوع و تعداد اتمهای آنها برابر اما ساختارهای متفاوتی دارند را ایزومر گویند.
ب)آیا خواص فیزیکی و شیمیایی آنها یکسان است؟ چرا؟
خیر – دو ترکیب گروههای عاملی متفاوت و در نتیجه خواص متفاوتی خواهند داشت. اولی دارای گروه عاملی هیدروکسیل و گروه عاملی آلکنی و دومی دارای گروه عاملی آلدهیدی است.
پ)آیا محتوای انرژی آنها را یکسان پیشبینی میکنید؟ توضیح دهید.
خیر – ساختار متفاوتی دارند. محتوای انرژی یک ترکیب در دما و فشار ثابت افزون بر نوع و تعداد اتمها به نحوه اتصال آنها و نوع پیوندهای شیمیایی آنها نیز مربوط است.
جواب خود را بیازمایید صفحه 71 شیمی یازدهم
1- با توجه به جدول 6 کتاب درسی آنتالپی سوختن پروپان (C3H8 )و 1ــ بوتن (C4H8 )را پیشبینی کرده سپس با مراجعه به منابع علمی معتبر درستی پیشبینی خود را بررسی کنید.
اختالف آنتالپی سوختن اتان و پروپان که در یک CH2 با هم تفاوت دارند برابر 670 -است. پروپان و اتان نیز در یک CH2 تفاوت دارند پس اختلاف آنتالپی سوختن آنها نیز2230- است. به همین ترتیب برای 1-بوتن میتوان نوشت که اختلاف آنتالپی آن 2706- است.
در منابع علمی معتبر برای پروپان 2219/2. برای 1-بوتن -2717 است.
2- با توجه به معادلۀ واکنش سوختن کامل اتان و اتانول به پرسشهای مطرح شده پاسخ دهید.
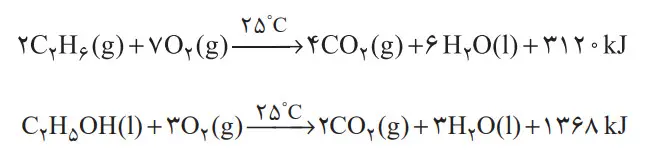
الف) ارزش سوختی هریک را محاسبه و با یکدیگر مقایسه کنید.
ارزش سوختی منظور از گرمای آزاد شده به ازای 1 گرم است.

ب) جرم CO2حاصل از سوختن یک گرم از هریک را محاسبه و با یکدیگر مقایسه کنید.
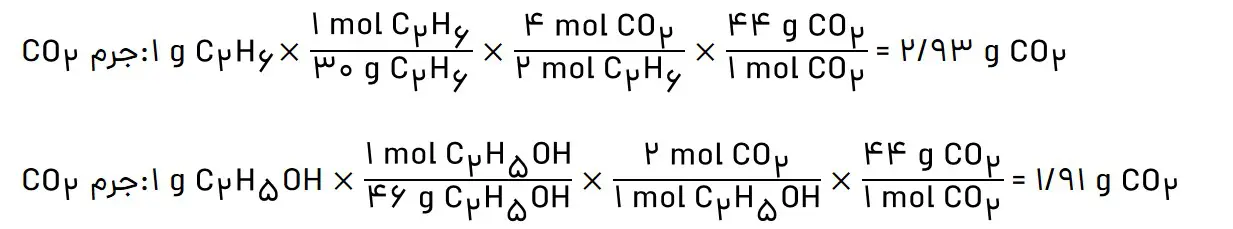
پ) توضیح دهید چرا اتانول سوخت سبز به شمار میرود؟
- در سوختن اتانول آلاینده و گاز گلخانهای کمتری تولید میشود. زیرا به ازا سوختن یک گرم اتانول، کربن دی اکسید کمتری حاصل میشود.
- اکسیژن کمتری مصرف میشود.
- علاوه بر آن اتانول از بقایای گیاهانی مانند نیشکر، سیب زمینی و ذرت تهیه میشود که منابع تجدیدپذیر هستند.
جواب خود را بیازمایید صفحه 74 شیمی یازدهم
هیدروژن پراکسید (H2O2) مادهای است که با نام تجاری آب اکسیژنه به فروش میرسد.
الف) با استفاده از واکنشهای داده شده، آنتالپی واکنش زیر را حساب کنید.
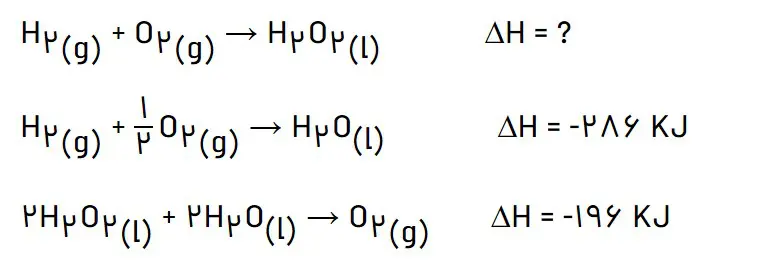
با توجه به قانون هس واکنش اول را مینویسیم و واکنش دوم را برعکس نموده و در 1/2 ضرب میکنیم. در نتیجه آنتالپی واکنش اول تغییر نمیکند و آنتالپی واکنش دوم تقسیم بر 2 میشود.
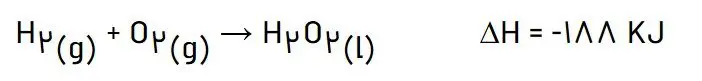
ب) توضیح دهید چرا تهیه این ماده از واکنش مستقیم گاز هیدروژن با اکسیژن ممکن نیست؟
آب ترکیب پایدارتری نسبت به آب اکسیژنه است، به همین جهت از ترکیب گازهای هیدروژن و اکسیژن آب حاصل میشود و نمیتوان آب اکسیژنه را از ترکیب این دو گاز بدست آورد.
2- در شیمی 1 آموختید که گازهای آلاینده مانند NO و CO از اگزوز خودروها به هواکره وارد میشوند. شیمیدانهای هواکره انجام واکنش زیر را برای تبدیل این آلایندهها به گازهایی پایدارتر و با آلایندگی کمتر، طراحی کردهاند.
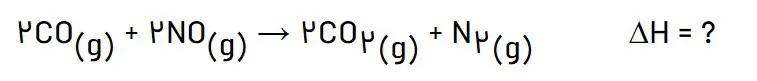
آنتالپی واکنش بالا را با استفاده از واکنشهای ترموشیمیایی زیر حساب کنید.
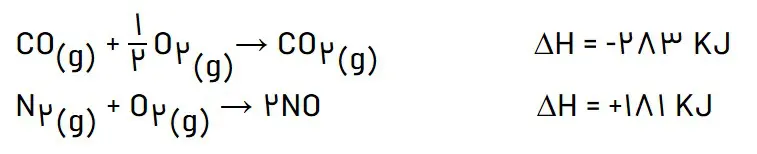
واکنش اول را در دو ضرب میکنیم و واکنش دوم را معکوس میکنیم تا آنتالپی واکنش خواسته شده به دست آید.
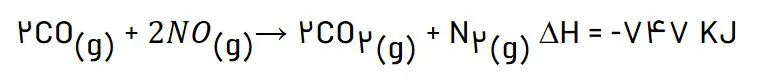
در مقاله جواب تکمیل کنید دینی یازدهم پاسخ کامل این قسمت از کتاب دینی یازدهم را بدون نیاز به منابع دیگر مشاهده کنید.
3- واکنش سوخنت کامل گرافیت را میتوان مجموعهای از دو واکنش پیدرپی مطابق نمودار زیر دانست.
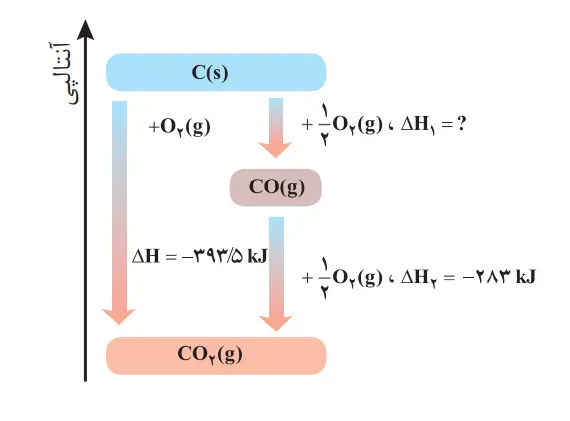
الف) شواهد نشان میدهد که H∆ واکنش تولید COg را نمیتوان به روش تجربی تعیین کرد. درباره علت آن گفتوگو کنید.
گاز CO2 پایدارتر از گاز CO است به همین جهت از واکنش گرافیت با گاز اکسیژن محصول پایدارتر کربن دی اکسید حاصل میشود.
ب) H∆ واکنش تولید COg را از گرافیت و گاز اکسیژن حساب کنید.
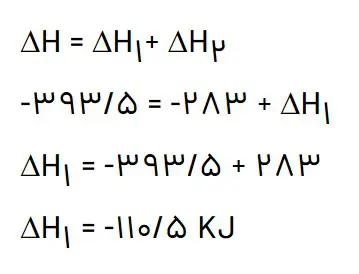
4- شواهد تجربی نشان میدهند که تهیە آمونیاک به روش هابر از گازهای نیتروژن و هیدروژن مطابق نمودار زیر یک واکنش دو مرحلهای است.
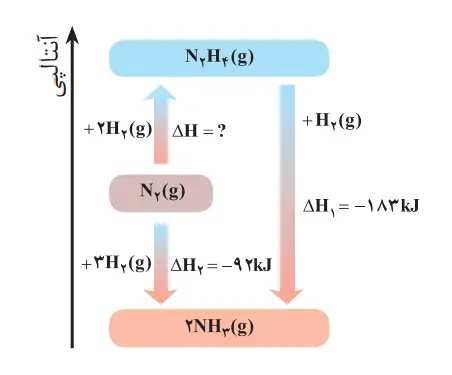
الف) در شرایط یکسان، هیدرازین پایدارتر است یا آمونیاک؟ چرا؟
آمونیاک پایدارتر از هیدرازین است. زیرا محتوای انرژی آن پایینتر از هیدرازین است.
ب) آنتالپی واکنش تولید هیدرازین را حساب کنید.
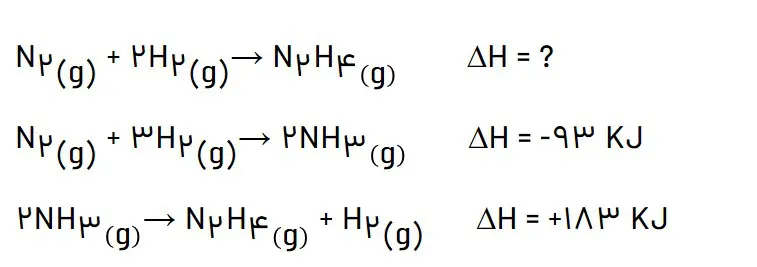
با توجه به قانون هس:
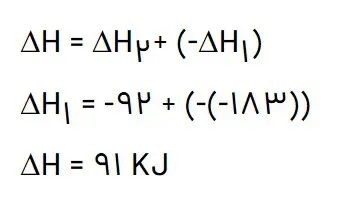
جواب خود را بیازمایید شیمی یازدهم صفحه 76
هر یک از موارد زیر نقش چه عاملی را در سرعت واکنش نشان میدهد؛ توضیح دهید.
الف) برای نگهداری طولانیمدت فراوردههای گوشتی و پروتئینی، آنها را به حالت منجمد ذخیره میکنند.
نقش دما با کاهش دما سرعت واکنش کم میشود.
ب) روغنهای مایع که در ظرف مات و کدر بستهبندی شدهاند، زمان ماندگاری بیشتری دارند.
نقش نور. نور انرژی لازم جهت انجام فرایند فساد روغن را فراهم میکند.
ث) قاووت گردی مغذی و تهیه شده از مغز آفتابگردان، پسته و … است. این سوغات کرمان زودتر از مغز این خوراکیها فاسد میشود.
در گرد قاووت سطح تماس با اکسیژن هوا بیشتر از مغز سالم است لذا فرایند فساد با سرعت بیشتری رخ میدهد.
در آموزش فصل اول زیست یازدهم | تنظیم عصبی کاملترین آموزش این فصل را همراه با نکات کنکوری را مطالعه کنید.
جواب خود را بیازمایید شیمی یازدهم صفحه 80
در هر یک از موارد زیر با توجه به شکل، علت اختلاف در سرعت واکنش را توضیح دهید.
الف) فلزهای قلیایی سدیم و پتاسیم در شرایط یکسان با آب سرد به شدت واکنش میدهند، اما سرعت واکنشها متفاوت است.

واکنشپذیری پتاسیم بیشتر از سدیم است. واکنشپذیری در گروه فلزات قلیایی با افزایش عدد اتمی افزایش مییابد.
ب) آتش، گردِ آهن موجود در کپسول چینی را داغ و سرخ میکند؛ در حالی که شعله پاشیدن و پخشکردن گردِ آهن بر روی شعله، سبب سوختن آن میشود.

در گرد آهن سطح تماس واکنشدهندهها بیشتر است و سرعت واکنش بیشتر است.
پ) محلول بنفش رنگ پتاسیم پرمنگنات با یک اسید آلی در دمای اتاق به کندی واکنش میدهد اما با گرم شدن، محلول به سرعت بیرنگ میشود.

با افزایش دما سرعت واکنش افزایش مییابد به همین جهت سریعتر بیرنگ میشود.
ت)الیاف داغ و سرخ شده در هوا نمیسوزد، در حالی که همان مقدار الیاف آهن داغ و سرخ شده در یک ارلن پر از اکسیژن میسوزد.

با افزایش غلظت سرعت واکنش افزایش مییابد. ، به همین جهت الیاف آهن در اکسیژن خالص با سرعت بیشتری واکنش میدهند و نور و گرمای بیشتری ایجاد مینمایند.
ث) محلول هیدروژن پراکسید در دمای اتاق به کندی تجزیه شده و گاز اکسیزن تولید میکند، در حالی که افزودن دو قطره از محلول پتاسیم یدید، سرعت واکنش را به طور چشمگیری افزایش میدهد.

کاتالیزگر سرعت واکنش را افزایش میدهد، به همین جهت با افزایش پتاسیم یدید که نقش کاتالیزگر را دارد سرعت خروج گاز اکسیژن افزایش مییابد.
نمونه سوال فصل دوم شیمی یازدهم | در پی غذای سالم را باز کنید تا کاملترین و استانداردترین نمونه سوالات این فصل را به صورت رایگان و همراه با پاسخ کاملا تشزحی مشاهده بفرمایید.
جواب پیوند با ریاضی صفحه 82 شیمی یازدهم
یک تکه زغال چوب به شکل مکعب با طول ضلع 2 cm در نظر بگیرید. حجم این تکه زغال برابر باcm3 8، در حالیکه مساحت کل آن برابر با 24cm2 است (چرا؟).
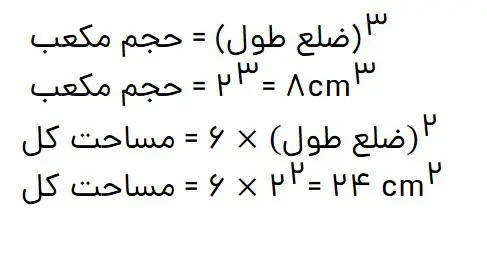
1- کدام کمیت (حجم یا مساحت کل)، سطح تماس این تکه زغال را با شعله هنگام سوختن نشان میدهد؟ توضیح دهید.
واکنش در سطح زغال که در تماس با اکسیژن است رخ میدهد.
2- اگر این مکعب از وسط یک ضلع برش بخورد و به دو مکعب مستطیل تقسیم شود، حساب کنید حجم زغال و سطح تماس آن چه تغییری میکند؟
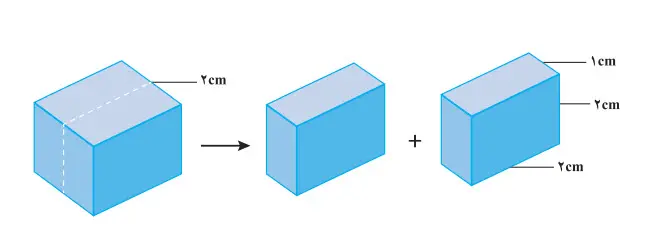
حجم زغال تغییری نمیکند. اما سطح افزایش مییابد.
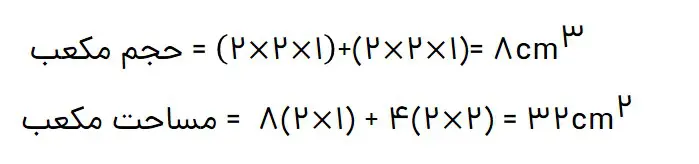
3- براساس تحلیل خود از پرسشهای بالا، علت تفاوت در سرعت واکنش سوختن تکە زغال با گرد آن را توضیح دهید.
با برش زغال در حجم ثابت، نسبت سطح به حجم افزایش مییابد. کمیت افزایش سطح به حجم باعث تقویت و یا تضعیف خواص ماده میشود.
جواب خود را بیازمایید صفحه 84 شیمی یازدهم
1- بر اساس شکل 14 کتاب درسی، آهنگ مصرف رنگ غذا را برحسب مول بر دقیقه حساب کنید.

2- دانشآموزی درون یک محلول محتوی 03/0 مول مس (II) سولفات، تیغهای از جنس روی قرار داده است. شکل زیر پیشرفت واکنش (Zn(s با (CuSO4 (aq را در این آزمایش نشان میدهد، با توجه به آن به پرسشها پاسخ دهید.

الف) واکنشپذیری فلز روی را با مس مقایسه کنید.
واکنشپذیری روی از مس بیشتر است.
ب) با گذشت زمان مقدار Cu(s)، Cu2+aq چه تغییری میکند؟ چرا؟
با گذشت زمان مقدار Cu 2+ aq کاهش و مقدار Cu s افزایش مییابد. زیرا اتمهای روی که فلز فعالتری است الکترون از دست داده و وارد محلول میشود و این الکترونها را یونهای مس جذب نموده و رسوب میکنند لذا از غلظت یونهای مس کم شده و به مقدار مس جامد افزوده میشود.
پ) اگر شمار مولهای مصرف شده از هر واکنشدهنده در واحد زمان بیانگر سرعت مصرف آن باشد، سرعت مصرف Cu 2+ aq را برحسب mol min -1 حساب کنید.
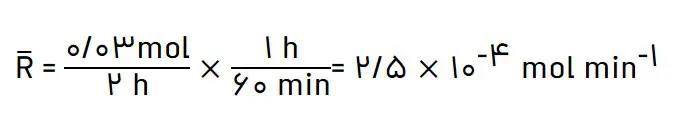
با هم بیندیشیم صفحه 85 شیمی یازدهم
واکنش کلسیم کربنات را با محلول هیدروکلریک اسید در دما و فشار اتاق مطابق شکل زیر در نظر بگیرید.
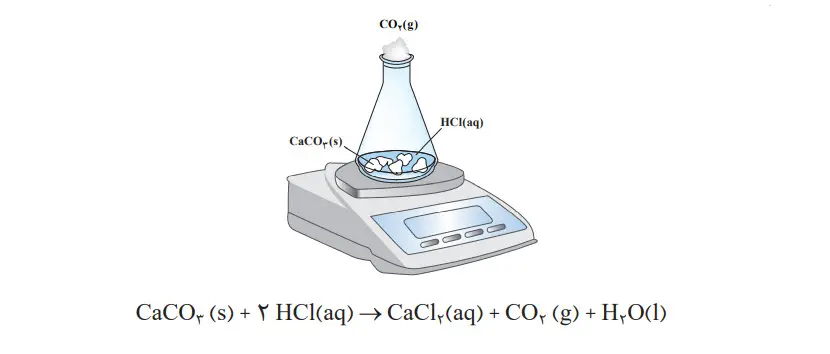
جدول زیر، جرم مخلوط واکنش را برحسب زمان برای این آزمایش نشان میدهد. با توجه به دادههای جدول، به پرسشهای مطرح شده پاسخ دهید:
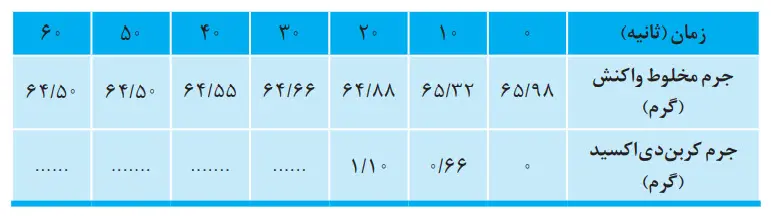
جواب تمرینهای آخر فصل کل کتاب شیمی یازدهم را میتوانید در لینک جواب تمرینهای دورهای شیمی یازدهم از فصل 1 تا 3 مشاهده کنید.
چرا با گذشت زمان از جرم مخلوط واکنش کاسته میشود؟
زیرا در طول واکنش گاز کربندیاکسید از محلول خارج میشود.
جدول را کامل کنید.

با گذشت زمان جرم گاز آزاد شده چه تغییری میکند؟ چرا؟
افزایش مییابد. زیرا کربن دی اکسید فراورده است و در طول واکنش تولید میشود.
در چه زمانی واکنش به پایان میرسد؟ چرا؟
50 ثانیه پس از شروع واکنش جرم محلول تغییری نکرده است پس واکنش پس از 50 ثانیه به پایان رسیده است.
2- جدول صفحه بعد را کامل کنید. (1mol CO2 = 44 g)
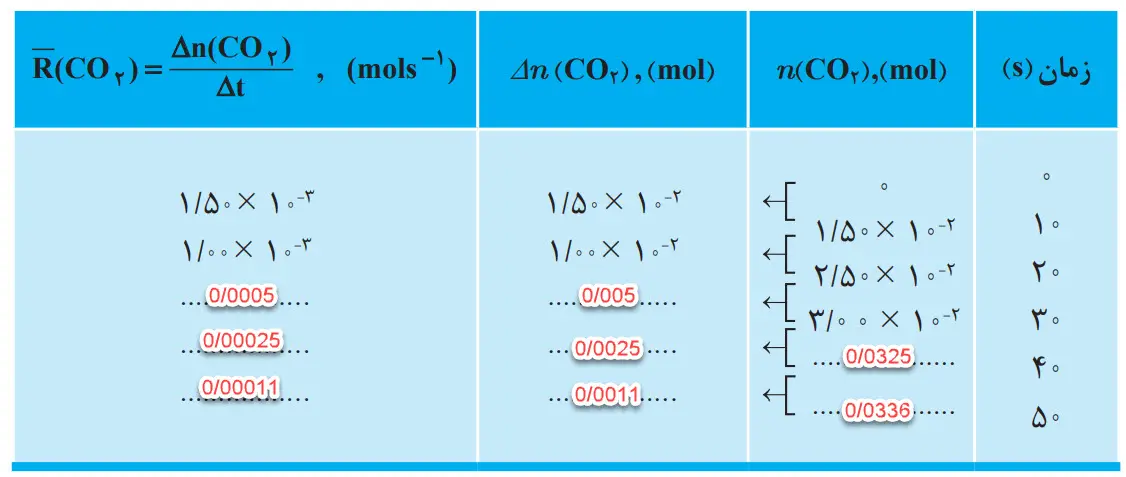
3- نمودار مول ــ زمان را برای گاز CO2 بر روی کاغذ میلیمتری زیر رسم کنید.
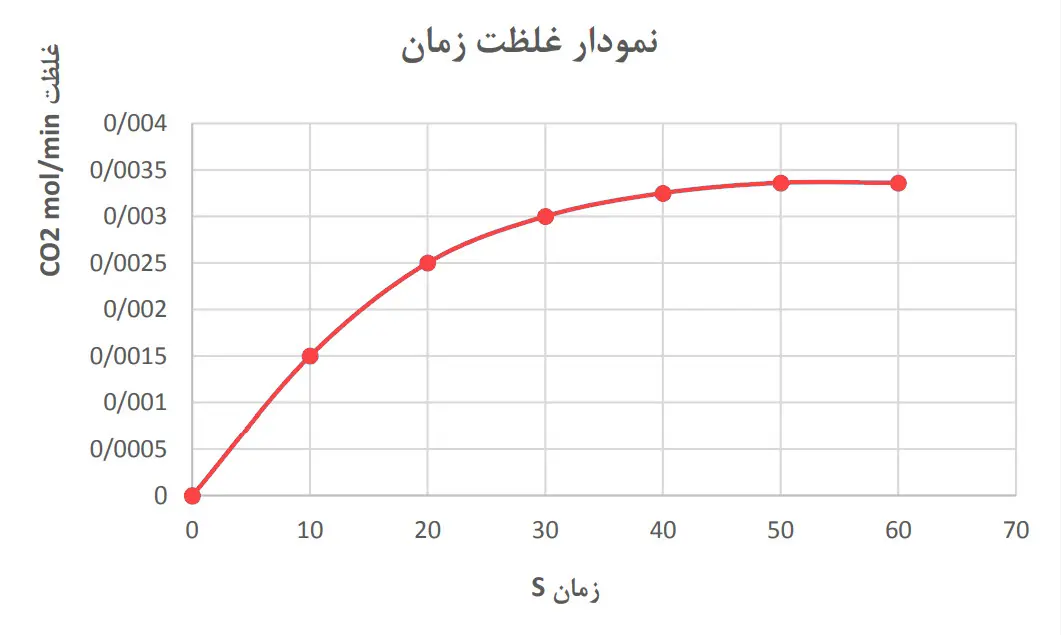
4ــ سرعت متوسط تولید CO2 با گذشت زمان چه تغییری میکند؟ چرا؟
کاهش مییابد، تغییرات غلظت گاز CO2 نسبت به زمان نشان میدهد که در بازههای زمانی برابر میزان تولید CO2 کاهش یافته است لذا میتوان نتیجه گرفت سرعت با گذشت زمان به علت کاهش غلظت واکنشدهندهها کاهش مییابد.
5- آزمایش نشان میدهد که نمودار مول ــ زمان برای هر سه فراورده در واکنش کلسیمکربنات با محلول هیدروکلریک اسید از هر لحاظ یکسان است. چرا؟
زیرا ضرایب استوکیومتری برای فراورده برابر است لذا به میزان برابر تشکیل میشوند.
جواب خود رابیازمایید شیمی یازدهم صفحه 87
1- در واکنش CaCO3 با HCl، چه رابطهای بین سرعت متوسط مصرف این دو ماده وجود دارد؟ این رابطه را بنویسید.
ضریب HCl دو و ضریب CaCO3 یک است پس میزان مصرف هیدروکلریک اسید دو برابر میزان مصرف کلسیم کربنات است و بنابراین:
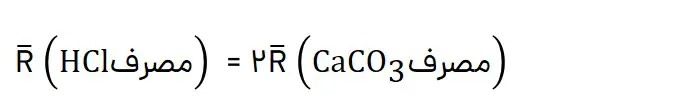
2- یکی از آلابندههای هوا که باعث تولید باران اسیدی میشود، گاز گوگردتریاکسید است که مطابق واکنش زیر تولید میشود:
(2SO2 (g) + O2(g) → 2SO3(g
اگر در شرایط معین سرعت متوسط اکسیژن 0/01 mol s-1 باشد، سرعت متوسط SO3 و SO2 را بر حسب 1ــ min mol حساب کنید.

3- با توجه به نمودار زیر که تغییر مولهای نوعی رنگ غذا در واکنش با یک محلول سفیدکننده را نشان میدهد، به پرسشهای مطرح شده پاسخ دهید.
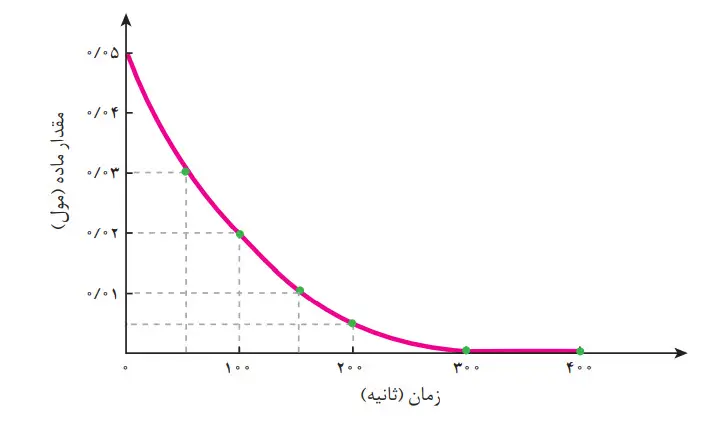
الف) مولهای واکنشدهنده (رنگ غذا) با گذشت زمان چه تغییری میکند؟ چرا؟
کاهش مییابد. زیرا رنگ غذا واکنشدهنده است لذا با گذشت زمان کاهش مییابد.
ب) شیب نمودار مول ــ زمان چه علامتی دارد؟ چرا؟
شیب نمودار منفی است. زیرا رنگ غذا واکنشدهنده است و با گذشت زمان کاهش مییابد.
پ) توضیح دهید چرا علامت منفی در رابطە زیر نوشته میشود.
تغییرات غلظت واکنشدهنده منفی است اما سرعت کمیتی مثبت است به همین جهت منفی گذاشته میشود تا منفی به مثبت تبدیل شود.
ت) سرعت متوسط مصرف رنگ غذا را برحسب مول بر دقیقه حساب کنید.
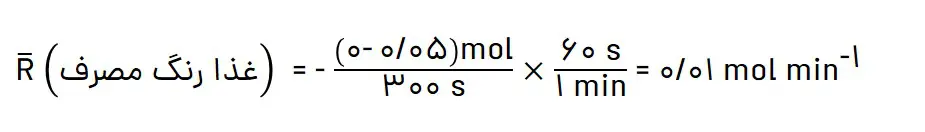
جواب خود رابیازمایید صفحه 89 شیمی یازدهم
در نمودار داده شده، منحنی A نشان دهندە تغییر مولهای یکی از مواد فراورده در واکنش فرضی است. با دلیل مشخص کنید کدام منحنی(BیاC)نشاندهنده افزودن بازدارنده و کدام یک نشان دهندە افزودن کاتالیزگر به سامانۀ واکنش است؟
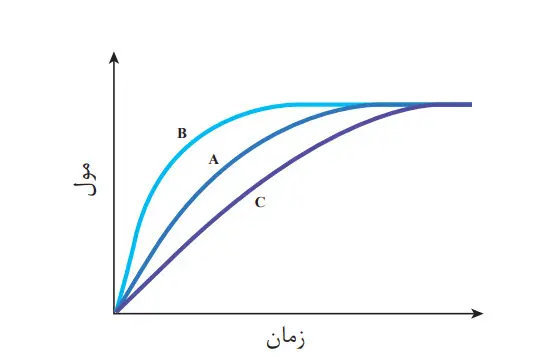
نمودار B افزودن کاتالیزگر است. با افزودن کاتالیزگر سرعت واکنش افزایش مییابد لذا تولید فراورده افزایش و شیب نمودار غلظت – زمان تندتر مییابد. نمودار C افزودن بازدارنده است. با افزودن بازدارنده سرعت واکنش کاهش مییابد لذا تولید فراورده کاهش و شیب نمودار غلظت – زمان کمتر میشود.
جواب باهم بیندیشیم صفحه 90 شیمی یازدهم
1- سرعت متوسط تولید گاز آمونیاک در شرایط معینی بر اساس معادله واکنش زیر در گسترە زمانی معینی برابر با 0/04 است.
(N2(g) + 3H2(g) → 2NH3(g
الف) سرعت متوسط مصرفN2 و H2 را در این گسترۀ زمانی حساب کنید.
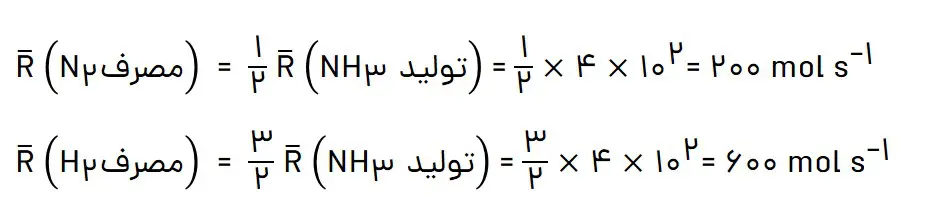
ب) سرعت متوسط تولید یا مصرف هر شرکتکننده را به ضریب استوکیومتری آن تقسیم کنید. از حاصل این تقسیمها چه نتیجهای میگیرید؟
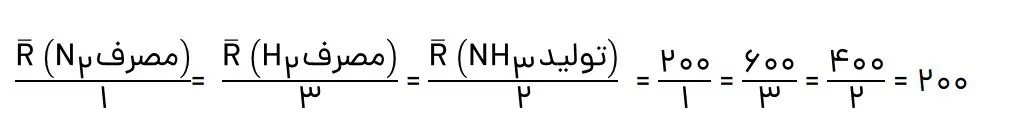
پ) حاصل تقسیم در قسمت ب، سرعت واکنش نام دارد. برای این واکنش با استفاده از سرعت متوسط تولید یا مصرف مواد شرکتکننده، رابطە سرعت واکنش را بنویسید.
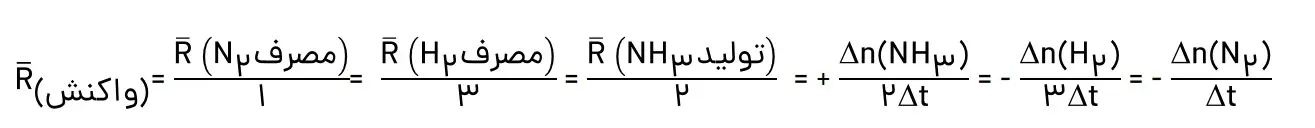
ت) ارتباط معادلۀ شیمیایی موازنه شده واکنش را با رابطە زیر توضیح دهید.
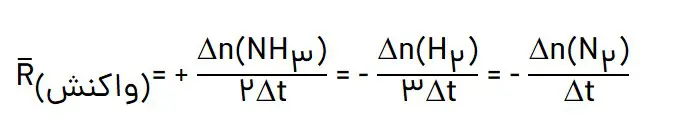
ث) سرعت متوسط کدام ماده با سرعت واکنش برابر است؟ توضیح دهید.
سرعت اجزایی از واکنش که ضریب استوکیومتری برابر یک دارند با سرعت متوسط واکنش برابر است.
2- قند موجود در جوانه گندم (مالتوز) مطابق واکنش زیر به گلوکز تبدیل میشود.
(C12H22O11(aq) + H2O(l) → 2C6H12O6(aq
این واکنش در دمای ثابت و شرایط معنی بررسی شده و جدول زیر، دادههای تجربی آن را نشان میدهد. با توجه به آن و نمودار داده شده، به پرسشهای زیر پاسخ دهید.
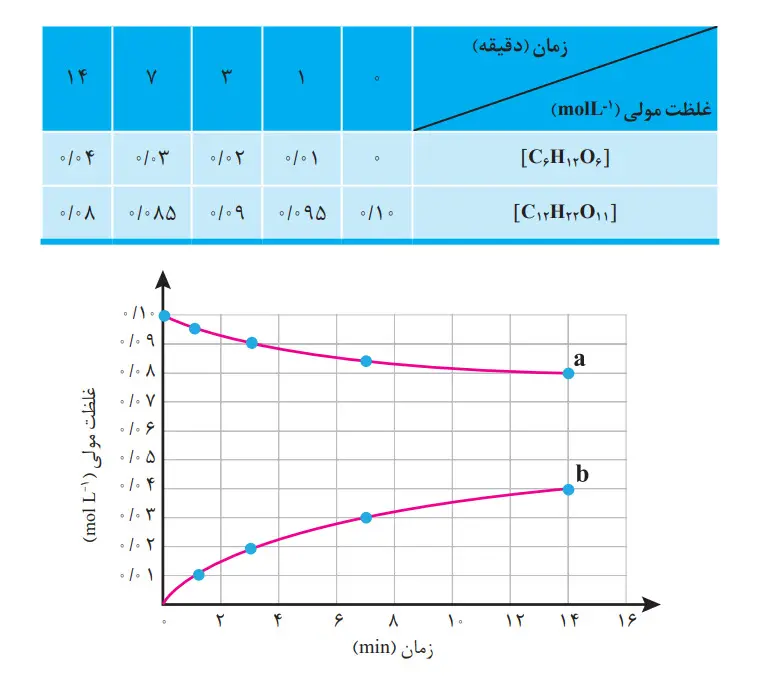
الف) در سه دقیقۀ نخست، (گلوکز)R و (مالتوز)R را برحسب mol L-1 s-1 حساب کنید.
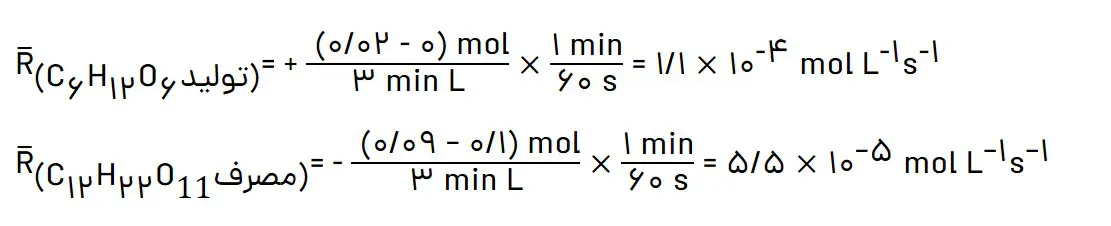
ب) سرعت واکنش را در هفت دقیقه نخست و هفت دقیقه دوم حساب کنید. کدام یک بیشتر است؟ چرا؟
سرعت واکنش برابر با سرعت مصرف مالتوز است زیرا ضریب استوکیومتری آن برابر یک است.
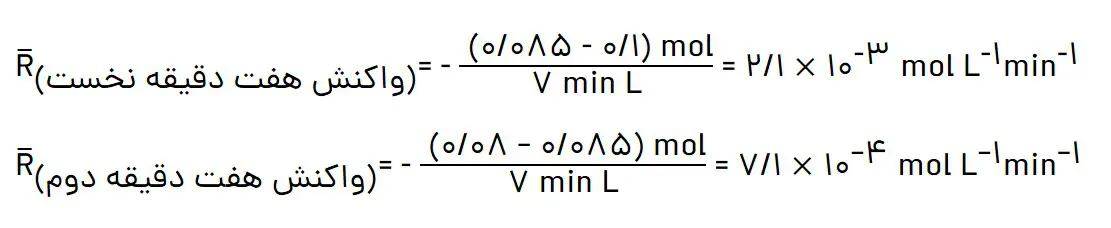
سرعت در هفت دقیقه نخست بیش تر است زیرا با گذشت زمان از غلظت واکنش دهنده ها کاسته شده سرعت
نیز کاهش می یابد
پ) هر یک از منحنیهای a و b مربوط به کدام ماده شرکتکننده است؟ توضیح دهید.
a مربوط به مالتوز است زیرا با گذشت زمان در حال کاهش است و شیب نمودار منفی است.
b مربوط به گلوکز است زیرا با گذشت زمان در حال افزایش است و شیب نمودار مثبت است به علاوه شیب نمودار آن بیشتر است؛ زیرا ضریب استوکیومتری بیشتر و شیب تندتری دارد.
جواب خود را بیازمایید صفحه 93 شیمی یازدهم
ستون سمت راست در جدول زیر چهار الگو برای کاهش ردپای غذا را نشان میدهد. در گفتوگو با یکدیگر مشخص کنید هر بیانی از اصل شیمی سبز در ستون سمت چپ با کدام الگو همخوانی بیشتری دارد.
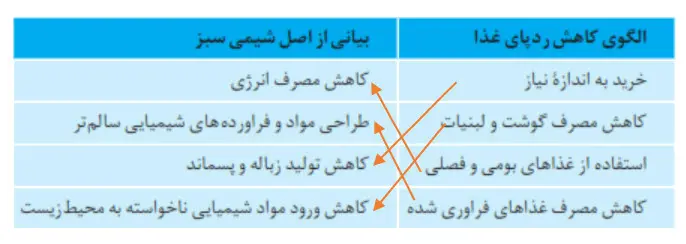
جواب تمرینهای دورهای شیمی یازدهم فصل دوم
1- اغلب ورزشکاران برای درمان آسیبدیدگیهای خود از بستههایی استفاده میکنندکه به سرعت گرما را انتقال میدهند. اساس کار این بستهها، انحلال برخی ترکیبهای یونی در آب است. با توجه به معادلههای ترموشیمیایی زیر به پرسشهای مطرح شده پاسخ دهید:
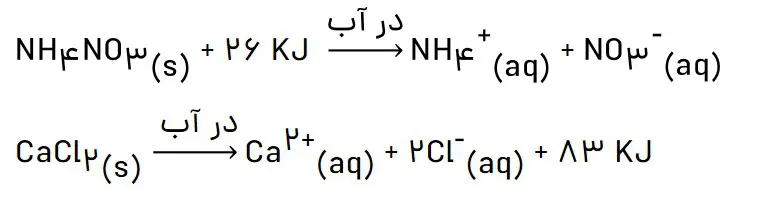
الف) کدام فرایند انحلال برای سرد کردن محل آسیبدیدگی مناسب است؟ چرا؟
واکنش اول؛ چون گرماگیر است و با جذب گرما از محل آسیبدیده آن را سرد میکند.
ب) از انحلال کامل g 2/22 کلسیم کلرید خشک درآب چند کیلوژول گرما آزاد میشود؟
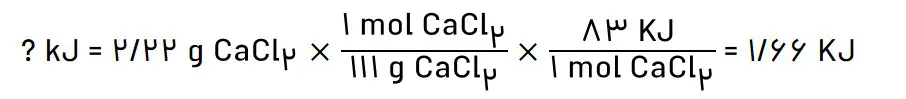
2- چربی ذخیره شده در کوهان شتر هنگام اکسایش افزون بر آب مورد نیاز، انرژی لازم برای فعالیتهای جانور را نیز تامین میکند. واکنش ترموشیمیایی آن به صورت زیر است:
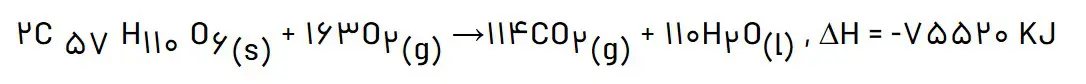
حساب کنید از اکسایش هر کیلوگرم چربی، چند کیلوژول انرژی آزاد میشود؟
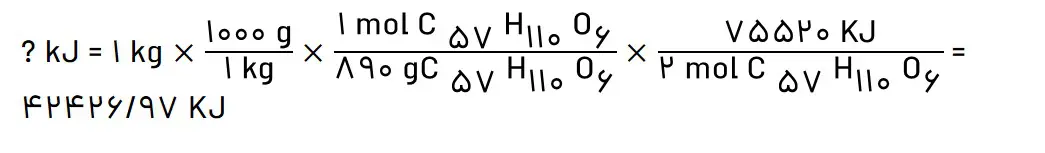
3- کلسترول، یکی از مواد آلی موجود در غذاهای جانوری است که مقدار اضافی آن در دیوارە رگها رسوب میکند، فرایندی که منجر به گرفتگی رگها و سکته میشود. با توجه به ساختار آن به پرسشهای مطرح شده پاسخ دهید.
الف) توضیح دهید چرا شیمیدانها آن را یک الکل سیر نشده میدانند؟
چون در ساختار این مولکول، علاوه بر گروه عاملی الکلی (هیدروکسیل) یک پیوند دوگانه کربن کربن وجود دارد.
ب) با توجه به جدول شمارۀ 3، در شرایط یکسان کدام پیوندهای اشتراکی یگانه در ساختار کلسترول آسانتر شکسته میشود؟ چرا؟
با توجه به مقادیر آنتالپی پیوند در جدول شماره 3، پیوند ساده کربن-کربن مقدار انرژی کمتری برای شکسته شدن نیاز دارد و آسانتر شکسته میشود.
4- از مصرف هر گرم آلومینیم در واکنش ترمیت، kJ 24/15 گرما آزاد میشود.
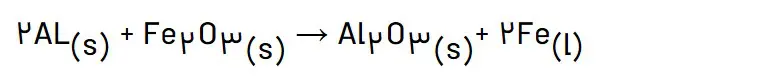
الف) این مقدار گرما، دمای صدگرم آب خالص را چند درجۀ سلسیوس افزایش میدهد؟
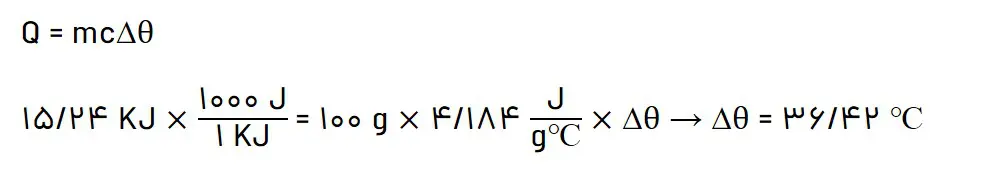
ب) ΔH واکنش ترمیت را حساب کنید.
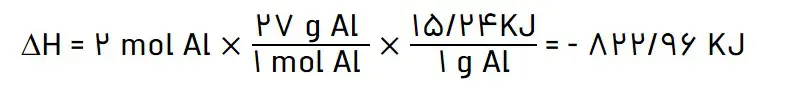
5- با توجه به واکنش ترموشیمیایی داده شده، آنتالپی واکنش خواسته شده را حساب کنید. (راهنمایی: آنتالپی فرازش ید را 62/5 KJ mol-1 در نظر بگیرید).
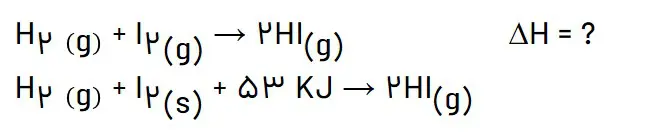
طبق قانون هس واکنش داده شده را تغییر نمیدهیم و واکنش فرازش ید را در منفی 1 ضرب میکنیم:
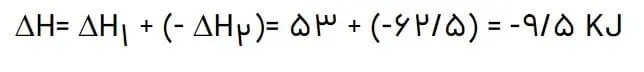
6- شکل زیر واکنش میان گاز هیدروژن و بخار بنفش رنگ ید را در دمای معینی نشان میدهد.

اگر هر ذره هم ارز با 0/1 مول از ماده و سامانه دو لیتری باشد، سرعت واکنش را پس از 20 دقیقه (b) و پس از 40 دقیقه (c) بر حسب mol L-1 h-1حساب و با یکدیگر مقایسه کنید.
در 20 دقیقه نخست واکنش، دو مول هیدروژن مصرف شده است. پس تغییر مول هیدروژن به صورت زیر است:
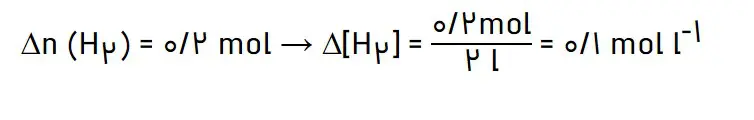
چون ضریب H2 در این واکنش برابر 1 است، پس سرعت متوسز مصرف هیدروژن با سرعت واکنش برابر است.
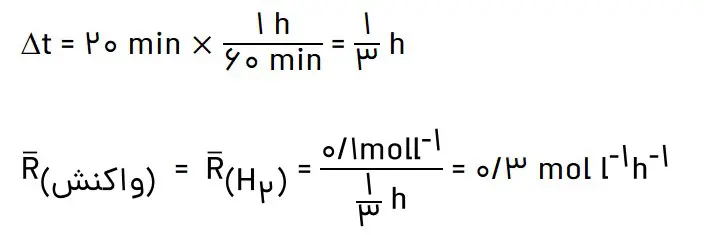
پس از 40 دقیقه:
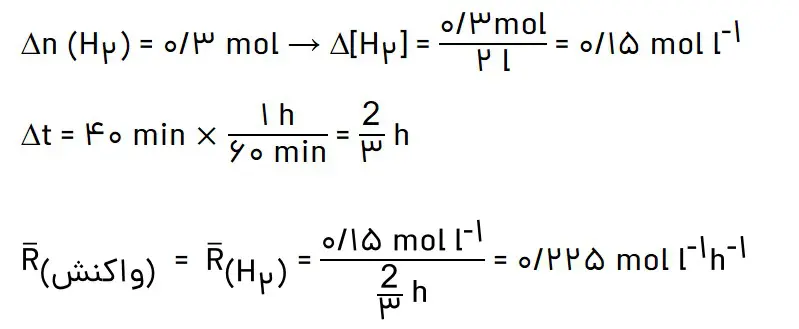
7- الف) H∆ واکنش زیر را با استفاده از جدول 2 و3 حساب کنید.
![]()
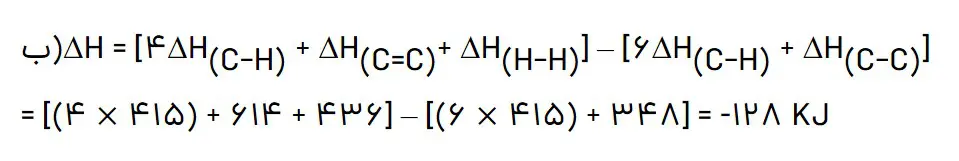
ب) آنتالپی سوختن اتن، اتان و هیدروژن که به ترتیب برابر با 1410،-1560 -و 286 -کیلو ژول بر مول است، حساب کنید.
معادله واکنش سوختن کامل این سه ماده به صورت زیر است:
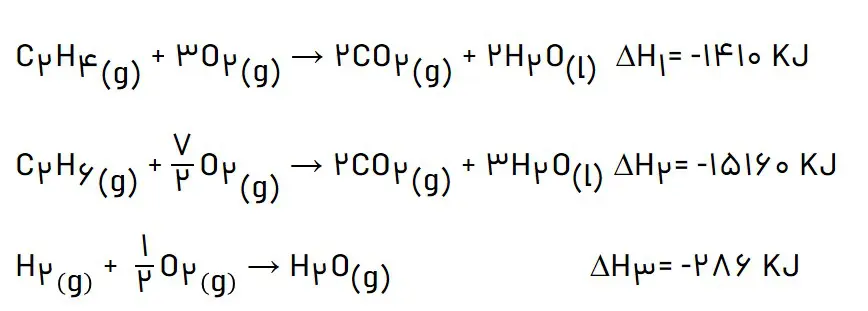
برای رسیدن به واکنش تهیه اتان از اتناید واکنش اول و سوم بدون تغییر و واکنش دوم برعکس شود. بنابراین آنتالپی واکنش به صورت زیر خواهد بود:
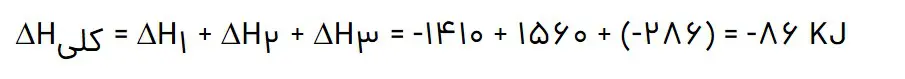
پ) ΔH محاسبه شده از کدام قسمت را برای یک گزارش علمی انتخاب میکنید؟ توضیح دهید.
محاسبات نشان میدهد که مقدار H∆ محاسبه شده به روش آنتالپی پیوند با مقدار اندازهگیری شده به روش تجربی تفاوت دارد و با خطای بیشتری همراه است. بنابراین آنتالپی واکنش بر حسب واکنش سوختن که خطای کمتری دارد انتخاب میشود.
8- با توجه به جدول زیر به پرسشهای مطرح شده پاسخ دهید.
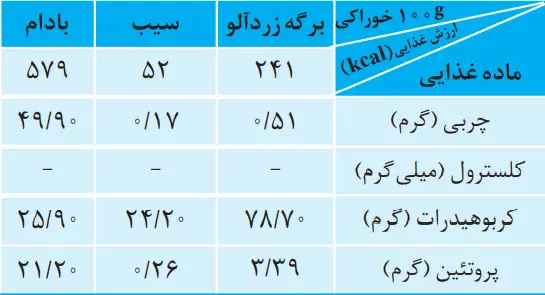
الف) اگر بدن فردی نیاز فوری و ضروری به تأمین انرژی داشته باشد، کدام خوراکی را پیشنهاد میکنید؟ چرا؟
برگه زردآلو. چون مقدار کربوهیدرات موجود در آن بیشتر است و زودتر تولید انرژی میکند.
ب) مصرف کدام خوراکی را برای فعالیتهای فیزیکی که در مدت طولانیتری انجام میشوند، مناسب میدانید؟ توضیح دهید.
بادام زمینی. زیرا میزان چربی موجود در آن بیشتر است و چربیها در مدت زمان طولانیتری در سوختوساز شرکت میکنند و کم کم انرژی خود را از دست میدهند.
پ) اگر یک فرد 70 کیلوگرمی، 25 گرم بادام خورده باشد، برای مصرف انرژی حاصل از آن چه مدت باید پیادهروی کند؟ آهنگ مصرف انرژی در پیادهروی را 190 Kcal h-1 در نظر بگیرید.
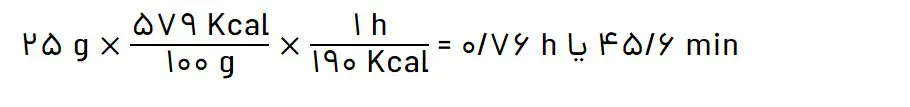
ایستگاه آخر
خب دوستان عزیزم به پایان مقاله گام به گام فصل دوم شیمی یازدهم رسیدیم و همانطور که قول داده بودم کاملترین پاسخها برای این بخش را در اختیار شما عزیزان قرار دادم و همه مطالب را بررسی کردم. برای مطالعه سایر مقالات مرتبط با شیمی یازدهم، از طریق لینک قرار داده شده اقدام کنید و برای مطالعه سایر مقالات دروس آموزشی، گام به گام و نمونه سوال، لینک یازدهم را دنبال نمایید.
در پایان هر سوالی که در رابطه با درس شیمی و جواب سوالات فصل دوم شیمی یازدهم دارید میتوانید از طریق نظرات با ما در میان بگذارید تا سریعا پاسخ دهم؛ با امتیاز دادن به این مقاله و عضویت در خبرنامه هم به شدت به ما برای نوشتن مطالب بیشتر روحیه خواهید داد.
سوالات متداول
- نمونه سوالات فصل دوم شیمی یازدهم را از کجا میتوانم پیدا کنم؟
در سایت بخون بجز آموزش و گام به گام نمونه سوال همه فصلها قرار داده شده است. - گام به گام فصل دوم شیمی یازدهم شامل حل تمرینهای دورهای میشود؟
بله، جواب کل تمرینهای دورهای به صورت کامل در گام به گام فصل دوم شیمی یازدهم قرار داده شده است.






