در مقاله قبل آموزش فصل دوم شیمی دوازدهم آسایش و رفاه در سایه شیمی را به طور کامل همراه با تصاویر و فایل صوتی آموزشی بررسی کردیم. امروز در این مقاله به بررسی گام به گام فصل دوم شیمی دوازدهم رفاه و آسایش در سایه شیمی خواهیم پرداخت.
در فصل دوم شیمی دوازدهم با مبحث الکترو شیمی و انواع سلول الکترولیتی آشنا خواهید شد. مبحث الکتروشیمی یکی از مباحث مورد علاقه طراحان سوالات امتحانی است و یکی از منابع اصلی سوالات امتحانی در این فصل تمرینات و فعالیتهای کتاب درسی میباشد که برای کسب نمره بیست و درصد عالی در آزمونهای مختلف یادگیری و بررسی این سری از فعالیتهای کتاب درسی ضروری میباشد.
با اعمال تغییرات هر ساله در کتاب درسی، سوالات و فعالیتهای کتاب نیز دچار تغییر میشوند و برای بسیاری از دانش آموزان پیدا کردن منبعی بهروزرسانی شده برای گام به گام فصل دوم شیمی دوازدهم یکی از دغدغههای قابل ذکر است.
اما همراهان گرامی سایت بخون، برای دستیابی به بروزترین و کاملترین گام به گام فصل دوم شیمی دوازدهم نیازی به نگرانی نیست. من سالار احمدی در این مقاله قصد دارم به بررسی گام به گام فصل دوم شیمی دوازدهم به طور کامل همراه با پاسخ تمامی خود را بیازماییدهای فصل دوم شیمی دوازدهم بپردازم پس اگر به دنبال پاسخ فصل دوم شیمی دوازدهم هستید تا آخر این مقاله در سایت بخون همراه من باشید.
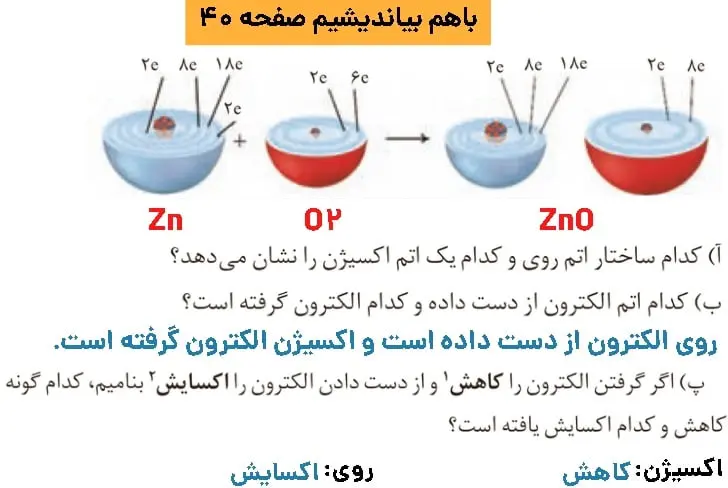
جواب باهم بیاندیشیم صفحه ۴۰ شیمی دوازدهم

جواب خود را بیازمایید صفحه ۴۲ شییمی دوازدهم

الف)
روی اکسایش یافته است، زیرا اتم روی الکترون از دست داده است و به کاتیون تبدیل شده است.
هیدروژن کاهش یافته است، زیرا اتم هیدروژن الکترون گرفته است و به آنیون تبدیل شده است.
ب)
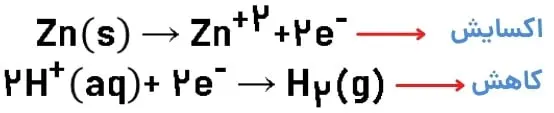
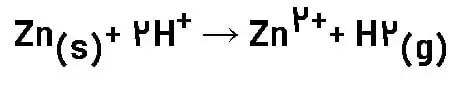
پ)

جواب خود را بیازمایید صفحه ۴۳ شیمی دوازدهم


پ)
فلز روی، هرچه تغییر دمای واکنش بیشتر باشد بدین معناست که در واکنش گرمای بیشتری آزاد شده و نشان دهنده تمایل بیشتر فلز برای از دست دادن الکترون است.
ت)
از چپ به راست به ترتیب بیشترین به کمترین: Zn-Fe-Cu-Au
ث)
خیر، زیرا قدرت کاهندگی مس از روی کمتر است و نمیتوانیم یونهای روی را به اتم روی کاهش دهیم.
جواب باهم بیاندیشیم صفحه ۴۵ شیمی دوازدهم


الف)
ب)
الکترود روی آند
الکترود مس کاتد
پ)
الکترونها از سمت آند به کاتد حرکت میکنند.
تمایل فلز روی بیشتر از فلز مس است، اتمهای روی در الکترود الکترون از دست میدهند و الکترونهای آزاد شده از طریق سیم(رابط خارجی) به سمت کاتد حرکت میکنند.
ت)
اتمهای روی در آند الکترون از دست میدهند و از تیفه جدا میشوند و به شکل یون بار ۲ مثبت وارد محلول میشوند و از جرم تیغه روی کاسته میشود.
یونهای دو بار مثبت مس در کاتد با گرفتن ۲ الکترون به شکل اتمهای مس بر سطح تیغه میچسپند، بنابراین بر جرم تیغه مس افزوده خواهد شد.
جواب خود را بیازمایید صفحه ۴۶ فصل دوم شیمی دوازدهم

پ)
اتم های مس در آند با از دست دادن الکترون اکسایش پیدا میکنند و از تیغه مس جدا میشوند و از جرم الکترود مس کم میشود.
یونهای نقر با یک بار مثبت الکترون دریافت میکنند و به اتم نقره تبدیل میشوند و بر سطح تیغه الکترود روی مینشیند و بر جرم الکترود نقره افزوده خواهد شد.
ث)
کاتیونها به سمت الکترو کاتد تیغه نقره و آنیونها به سمت الکترود آند تیغه مس حرکت میکنند.
جواب خود را بیازمایید صفحه ۴۸ شیمی دوازدهم

الف)
منیزیم آند و نقره کاتد است.
E0 منیزیم کمتر از نقره است،منیزیم کاهندهتر از نقره است و در جایگاه آند قرار میگیرد و نقره نیز کاتد خواهد بود.
جواب پیوند با ریاضی صفحه ۴۸ شیمی دوازدهم


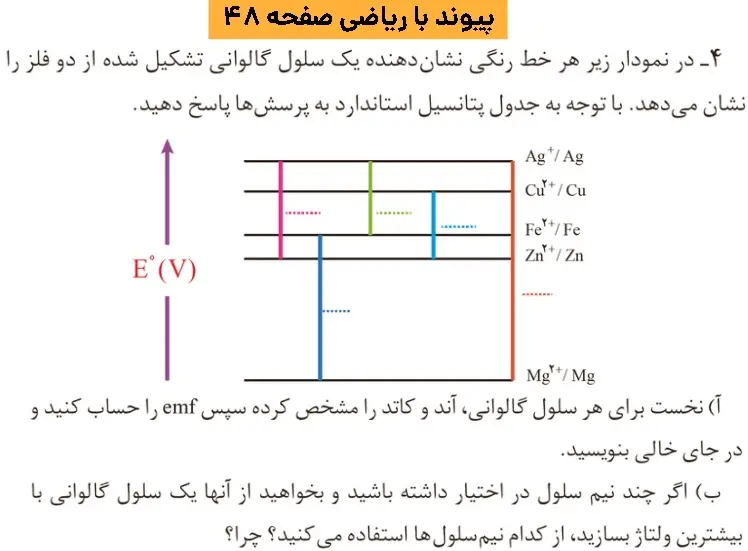
الف)

منیزیم(آند) – نقره(کاتد):
روی(آند) – مس(کاتد):
![]() آهن(آند) – نقره(کاتد):
آهن(آند) – نقره(کاتد):
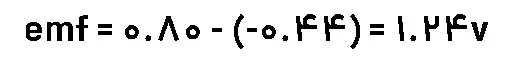 منیزیم(آند) – آهن(کاتد):
منیزیم(آند) – آهن(کاتد):
![]() روی(آند)– نقره(کاتد):
روی(آند)– نقره(کاتد):
![]() ب)
ب)
از منیزیم به عنوان آند و از نقره به عنوان کاتد استفاده میکنیم زیرا بیشترین اختلاف پتانسیل را دارند.

جواب خود را بیازمایید صفحه ۵۱ شیمی دوازدهم
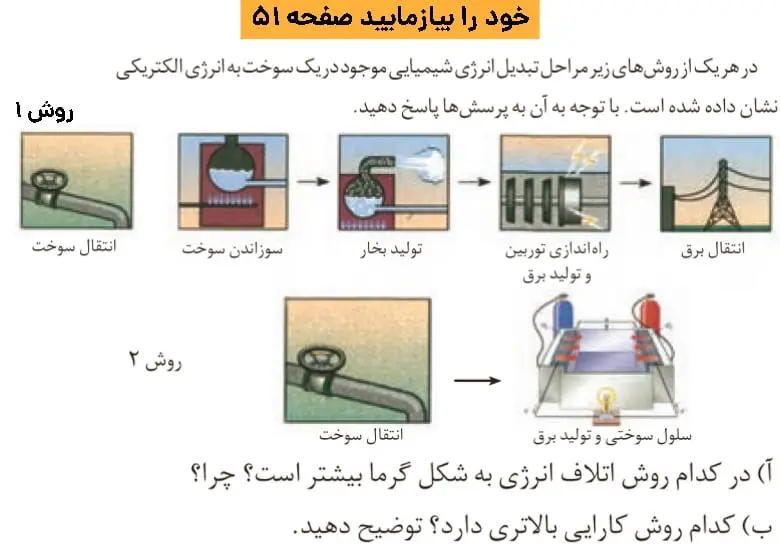
الف)
روش دوم (سلول سوختی) مراحل کمتری دارد و اتلاف انرژی گرمایی کمتری نیز دارد.
ب)
روش دوم به مراتب کارایی بالاتری دارد زیرا آلودگی کمتر و اتلاف وقت و انرژی کمتری دارد و درصد بیشتری از انرژی شیمیایی در سلول سوختی به انرژی الکتریکی تبدیل میشود و سوخت کمتری نیز مصرف میکند.
قسمت اول گام به گام فصل دوم شیمی دوازدهم
همراهان و دوستان گرامی به قسمت اول گام به گام فصل دوم شیمی دوازدهم رسیدیم. پیشنهاد میکنم پس از مطالعه کامل این مقاله برای یادگیری هرچه بهتر مفاهیم فصل دوم شیمی دوازدهم به بررسی نمونه سوالات فصل دوم شیمی دوازدهم بپردازید. در ادامه به بررسی تمرینات دورهای فصل دوم شیمی دوازدهم همراه با فعالیتهای کتاب خواهیم پرداخت.
جواب باهم بیاندیشیم صفحه ۵۲ فصل دوم شیمی دوازدهم
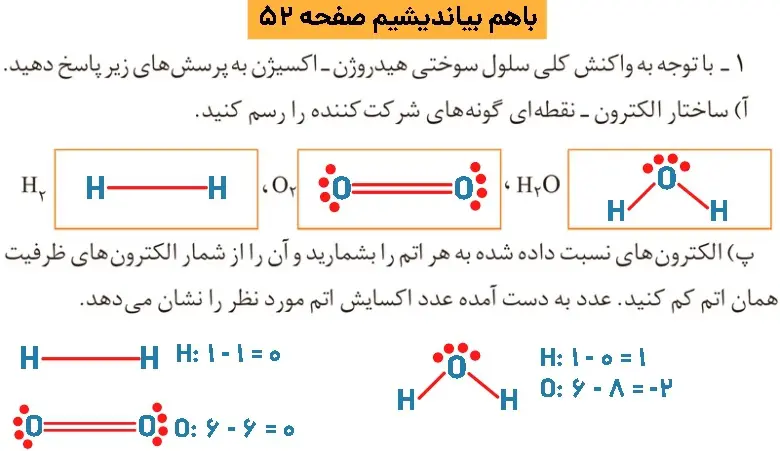

سوال۲)
هیدرون اکسایش یافته است و عدد اکسایش آن بیشتر شده است و اکسیژن کاهش یافته است و عدد آن کمتر شده است.
هیدروژن کاهنده و اکسیژن اکسنده است.
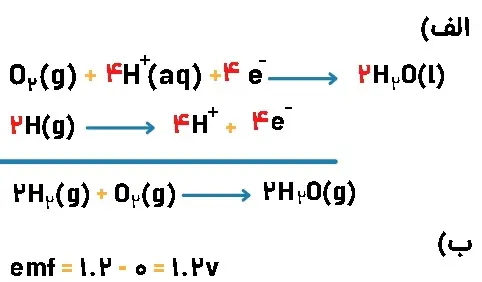

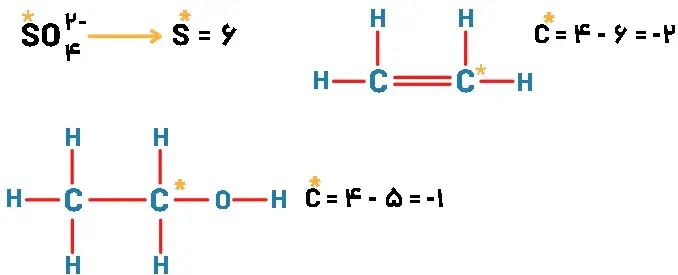
سوال۳)
عدد اکسایش کربن از ۴- به ۴+ افزایش پیدا کردهاست پس اکسایش یافتهاست و گونه کاهنده میباشد همچنین عدد اکسایش اکسیزن از ۰ به ۲- کم شده است پس کاهش یافته است و گونده اکسنده میباشد.
ب)
در سلول سوختی هیدروژن- اکسیژن تنها فراورده آن بخار آب است در حالی که در سلول سوختی متان علاوه بر بخار آب، کربن دیاکسید نیز تولید میشود که منجر به افزایش اثر گلخانهای میشود.
جواب خود را بیازمایید صفحه ۵۳ شیمی دوازدهم

جواب خود را بیازمایید صفحه ۵۴ شیمی دوازدهم

پ)
اطراف آند شناساگر به رنگ قرمز در میآید زیرا در پیرامون آند یون هیدرژون تولید میشود و در اطراف کاتد شناساگر به رنگ آبی نزدیک میشود زیرا در اطراف کاتد یوند هیدروکسید تولید میشود.
جواب خود را بیازمایید صفحه ۵۵ شیمی دوازدهم
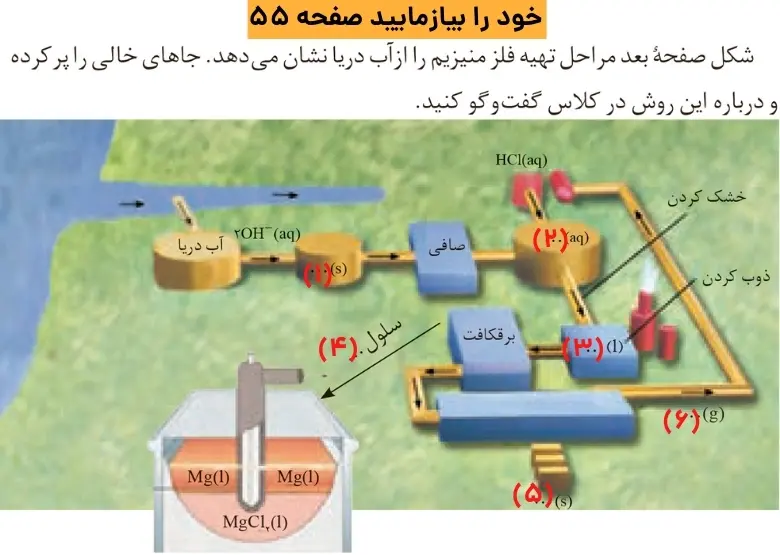
۱)
Mg(OH)2(s)
۲)
MgCl2(aq)
۳)
MgCl2(l)
۴)
سلول الکترولیتی
۵)
Mg(s)
۶)
Cl2(g)
جواب باهم بیاندیشیم صفحه ۵۷ شیمی دوازدهم

الف)
اگر به جرمی از آهن، به میزان کافی زمان بدهیم، در حضور آب و اکسیژن، به طور کامل به زنگ آهن تبدیل میشود. زنگ آهن در سطح خود به صورت پوستهپوسته و شکننده ظاهر میشود و هیچ حفاظتی را در برابر سطوح زیرین خود در برابر زنگ زدگی ایجاد نمیکند.

جواب خود را بیازمایید صفحه ۵۹ شیمی دوازدهم

پ)
حلبی برای بسته بندی مواد غذایی مناسبتر است زیرا فلز قلع با اسید میوه و مواد غذایی واکنش نخواهد داد اما آهن گالوانیزه با اسید میوه و مواد غذایی وارد واکنش میشود و منجر به فاسد شدن مواد غذایی میشود.
جواب خود را بیازمایید صفحه ۶۰ شیمی دوازدهم

پ)
از آنجایی که جنس روکش قاشق مورد نظر از نقره است، باید کاتیونهای موجود در محلول نیز نقره باشند تا با کاهش لایهای از سطح قاشق بر آن بنشینند.
جواب خود را بیازمایید صفحه ۶۲ شیمی دوازدهم

قاشق را در کاتد سلول الکتریکی قرار میدهیم و تیغهای از جنس نقره را در آند قرار داده و سپس محلول الکترولیت را یکی از نمکهای محلول نقره انتخاب میکنیم. در آند یونهای نقره از تیغه جدا میشوند و در کاتد بر سطح قاشق مینشینند.
جواب تمرینهای دورهای فصل دوم شیمی دوازدهم

الف)
فلز پلاتینیوم دارای پتانسیل کاهشی بالایی میباشد و در برابر اکسایش در حضور بیشتر فلزات مقاوم است.
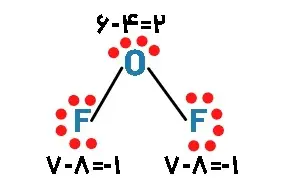
ب)
با توجه به شعاع و آرایش الکترونی اتم های فلوئور، تمایل این عنصر برای دریافت و یا از دست دادن الکترون بالا میباشد، بنابراین اکسنده ترین عنصر در جدول پتانسیل کاهشی عناصر است.
پ)
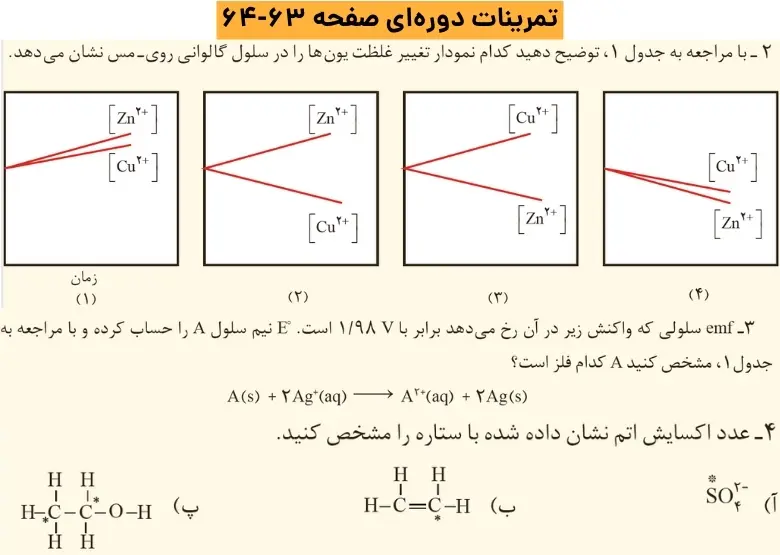
سوال ۲)
نمودار شماره(۲)
پتانسیل کاهشی مس بیشتر از روی است، بنابراین در سلول گالوانی مس کاتد و روی آند است. با گذشت زمان از غلظت یونهای دوبار مثبت مس در کاتد کم می شود و بر غلظت بونهای روی دوبار مثبت در آند افزوده میشود.
سوال ۳)
![]() فلز مورد نظر منگنز میباشد.
فلز مورد نظر منگنز میباشد.
سوال ۴)

سوال ۵)
الف)
اکسنده: اکسیژن کاهنده: نیتروژن
ب)
اکسنده: کلر کاهنده: ید
پ)
اکسنده: نیتروژن کاهنده: هیدروژن
سوال ۶)
الف)
اکسنده: نقره کاهنده: روی
ب)
آند: روی کاتد: نقره
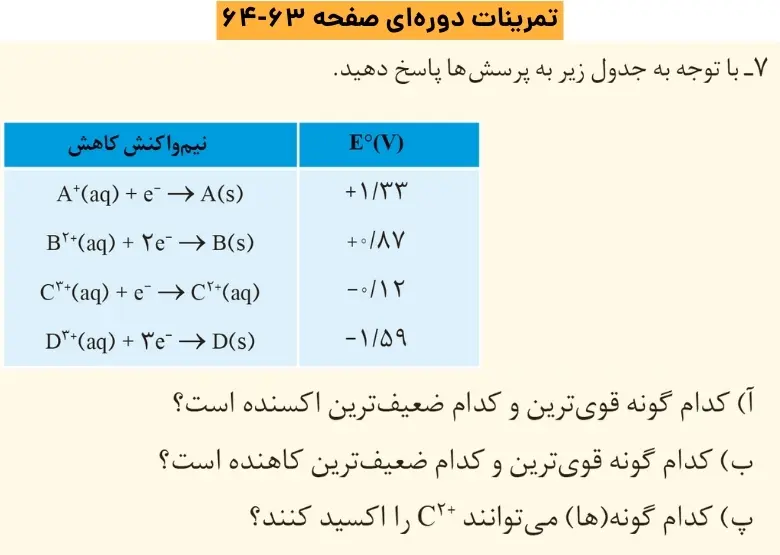
الف)
قویترین اکسنده: A+(aq)
ضعیفترین اکسنده: (aq)+D۳
ب)
قویترین کاهنده: (aq)+D۳
ضعیفترین کاهنده:(aq)+A
پ)
B2+(aq) -(aq)+A

سوال ۸)
قدرت اکسندگی:
Sn2+> Cr3+> Fe2+ x
فدرت کاهندگی:
Fe+> Cr2+> Sn
سوال ۹)
ظرف مسی، زیرا این ظرف مسی در مجاورت با اسید دچار خوردگی نمیشود و به عبارتی دیگر اتمهای اهن دارای پتانسیل کاهشی کمتری نسب به یونهای هیدروژن موجود در اسید هستند و دچار خوردگی میشوند اما با توجه به پتانسیل کاهشی مس در مقایسه با هیدروژن، ظرف مسی دچار خوردگی نمیشود.

الف)
نیم سلول آند:
SiO2(s)+ 4H+(aq) + 4e- → Si(s) + 2H2O(l)
نیم سلول کاتد:
2H2O(l) + 2e- → H2(g) + 2OH-(aq)
emf
emf=-0.83 -(-0.84) =+0.01v
ب)
زیرا گاز H2 گاز خطرناکی است و تحت کنترل تولید میشود.
خب دوستان و همراهان گرامی سایت بخون به انتها این مقاله از سری مقالههای گام به گام شیمی دوازدهم رسیدیم. در این مقاله سعی کردم تمایی خود را بیازمایید های فصل دوم شیمی دوازدهم را همگام با آخرین تغییرات کتاب درسی در سال ۱۴۰۰بررسی کنم. همچنین دوستان عزیز میتوانید از بخش پایه دوازدهم به مطالب زیر دسترسی پیدا کنید.
سوالات متداول جواب سوالات فصل دوم شیمی دوازدهم
- آیا گام به گام شیمی دوازدهم فصل دوم 1400 همگام با تغییرات جدید کتاب درسی شیمی دوازدهم میباشد؟
بله گام به گام فصل دوم شیمی دوازدهم همگام با آخرین تغییرات کتاب درسی است. - خود را بیازماییدهای اپدیت ۱۴۰۰ در گام به گام شیمی دوازدهم فصل دوم بررسی شده است؟
بله تمامی آپدیت های ۱۴۰۰ کتاب شیمی دوازدهم در گام به گام شیمی دوازدهم فصل دوم لحاظ شده است. - تمرینات دورهای به صورت کامل در گام به گام فصل ۲ شیمی دوازدهم بررسی شده است؟
بله سوالات جدید تمرینات دورهای هم به طور کامل در گام به گام فصل ۲ شیمی دوازدهم بررسی شده است.